治験管理室
くすりができるまで…
人間を対象にした研究に臨床研究があり、その中に臨床試験がありその中に治験が含まれています。
人の「有効性」や「安全性」について調べる試験を一般に「臨床試験」と呼んでいます。
厚生労働省から「薬」として承認を受けるために行う臨床試験のことを「治験」といいます。
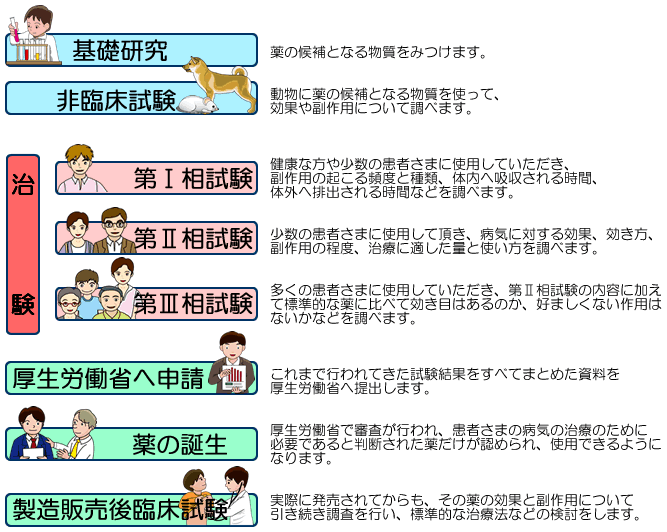
◆薬として販売されるまでには、次のようなステップを踏んでいます
治験に参加するには
一般に治験に参加する方々には、現在おかかりの病院、医院の主治医からの紹介、または新聞広告やポスターなどの広告による募集に参加する方法があります。
治験には病気の状態など参加していただける要件が決まっている場合があるので、参加できないこともあります。
治験を受ける流れ
治験に参加するまで
登録実施中の治験に関して、対象と思われる患者様に、医師からお話があります。
かかっている病気やその治療方針について、また治験に関することについて医師から説明を受けます。その後、臨床試験コーディネーターが治験について詳しく説明致します。
患者様は説明を受け、ご理解頂いた上で、治験を受けるかどうかをゆっくり決めて頂きます。
そして、同意文書などの手続きを踏み、治験開始となります。
尚、治験開始後のいつでも、患者様の意思で参加を止めることができます。
治験実施中の受診について
治験の正確なデータ(有効性・安全性)を得るためには、薬の使用方法を守り、定期的に受診して頂くことになります。
ただし、病状によっては、途中で治験を中止して適切な治療方法に変更することもあります。
臨床試験コーディネーターがサポート致します
受診時は、臨床試験コーディネーターが受け付けからお帰りまで同行し、スムーズに診察や検査などを受けて頂ける様、院内の調整を図ります。
薬や治験に関する説明を行う他、患者様やご家族の疑問や不安などについてもご相談を承ります。
健康成人を対象とした治験は行っておりません
当院では、健康成人を対象とした治験は行っておりません。
また、実施している施設のご紹介もしておりませんのでご了承願います。
治験関連文書は全試験電磁化対応しています。
次の項目について、Veeva Site Vaultを治験依頼者と共に活用しています。。
・文書の作成・授受・電子原本保管
・IRB資料の配布、審議の実施(現時点では初回審査資料のみ紙資料併用)
・IRB議事概要の作成と公開(Googleドライブ共有フォルダ)、議事録は院内紙資料

